Una solución es una mezcla homogénea que consta de dos o más sustancias, mientras que la solubilidad es la cantidad máxima de un compuesto o sustancia que se puede disolver en varios disolventes .
Muchas de las diversas soluciones que encontramos en la vida cotidiana incluyen un vaso de jarabe dulce. En un vaso de almíbar hay varios componentes, a saber, agua, almíbar y azúcar.
Si estos componentes se mezclan juntos hasta que los componentes constituyentes ya no sean visibles, entonces se convierte en una solución.
Al discutir la solución, la siguiente revisión adicional incluye la definición, propiedades, tipos y factores de la solución.
Definición de solución y solubilidad.

Solución
Una solución es una mezcla homogénea que consta de dos o más sustancias. Llamada solución debido a los componentes constituyentes de la solución.
En una solución hay solventes y solutos. Soluto (soluto) es una sustancia que forma una solución que tiene una cantidad menor en una solución. Mientras tanto, el solvente (solvente) es una sustancia que es más abundante que el soluto.
La composición de la sustancia marina en solución se expresa mediante la concentración de la solución. Mientras tanto, el proceso de mezclar un soluto y un solvente para formar una solución se llama disolución o solvatación.
Para comprender más sobre la solución, considere la siguiente imagen de ilustración.
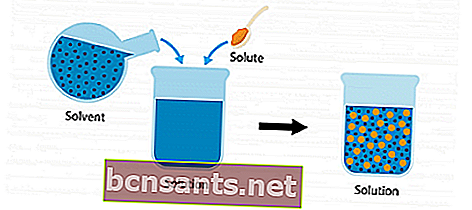
Hay un soluto y un solvente. Cuando los dos ingredientes se mezclan y combinan en un recipiente, se convierte en una solución.
Solubilidad (es)
La definición de solubilidad es la cantidad máxima de un compuesto o sustancia que se puede disolver en varios disolventes.
La solubilidad está simbolizada por s (solibilidad) en unidades mol / L o usualmente usa unidades de molaridad M. Aquí está la fórmula para solubilidad o molaridad.
M = n / V
donde M es la molaridad (mol / L), n es el número de moles de la sustancia (mol) y V es el volumen de la solución o disolvente (L).
La solubilidad también se define como la concentración de una sustancia que aún puede disolverse en una cierta cantidad de disolvente.
Producto de solubilidad constante (Ksp)
Un soluto disuelto en un solvente formará una reacción de equilibrio. La aparición del equilibrio está influenciada por solutos e iones de soluto insolubles.
Lea también: Más de 100 ejemplos de palabras estándar y no estándar + Explicaciones [ACTUALIZADO]El siguiente es un ejemplo de la constante de equilibrio para una reacción.
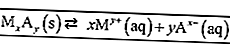
De acuerdo con las reglas para escribir la fórmula de equilibrio, solo las sustancias en forma de solución (aq) y gas (s) se escriben en la fórmula. Así que eso:
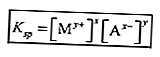
La constante de equilibrio para una solución que es difícil de disolver se llama constante del producto de solubilidad (Ksp).
Propiedades de la solución

Las propiedades físicas que aparecen en la solución se dividen en tres, a saber:
1. Propiedades coligativas de la solución
Es una característica de la solución que depende del número de partículas de soluto en una solución y no depende del tipo de partículas de disolvente.
Las propiedades coligativas son equivalentes a la concentración de diversas sustancias no electrolíticas en solución, independientemente del tipo o las propiedades químicas de los componentes.
Al determinar las propiedades coligativas de una solución de sólidos en un líquido, se considera que el sólido no es volátil y la presión de vapor por encima de la solución proviene completamente del solvente.
Algunas de las propiedades coligativas de una solución son la presión osmótica, disminución de la presión de vapor, aumento del punto de ebullición y disminución del punto de congelación.
2. Propiedades aditivas
En solución, las propiedades aditivas son propiedades de una solución que dependen del total de átomos en la molécula o del número de propiedades constituyentes de la solución.
Un ejemplo de las propiedades aditivas de las soluciones es el peso molecular, que es la suma de las masas atómicas.
La masa de los componentes de una solución se incluye en las propiedades aditivas, la masa total de la solución es la cantidad de cada componente de la solución, es decir, el soluto y el solvente.
3. Naturaleza constitutiva
Eso incluye la naturaleza de la solución que depende de los átomos de la molécula (del tipo de átomo y del número de átomos). Sus propiedades constitutivas indican las reglas de compuestos individuales y grupos de moléculas en el sistema.
Hay varias propiedades físicas que son en parte aditivas y constitutivas. Entre ellos se encuentran la refracción de la luz, las propiedades eléctricas, las propiedades superficiales e inter-superficiales que se incluyen en algunos constituyentes y en algunos aditivos.
Tipo de solución

1. Solución insaturada
Solución insaturada significa una solución que contiene menos soluto de lo necesario para hacer una solución saturada. Las soluciones insaturadas contienen partículas que no han reaccionado correctamente con la sustancia, en otras palabras, aún pueden disolver la sustancia.
Se dice que la solución está insaturada cuando el valor de concentración de iones <Ksp. En una solución insaturada no hay depósito de solutos.
Lea también: Definición de soluciones químicas y sus tipos y componentes.2. Solución saturada
Una solución se incluye en una solución saturada cuando hay un equilibrio entre el soluto y el solvente. En una solución saturada, las partículas reaccionan exactamente con el reactivo o experimentan una concentración máxima.
Se dice que la solución está saturada si la concentración de iones es la misma que el valor de Ksp. En esta condición de equilibrio, la velocidad del soluto en el solvente es la misma que la velocidad a la que se asienta. Es decir, la concentración de la sustancia en la solución es la misma.
3. Solución altamente saturada
Esa es una solución que contiene más soluto que el solvente. Esto hace que el valor del producto de la concentración de iones> Ksp de modo que la solución se sature y se asiente.
Factor de solubilidad

La solubilidad de un líquido varía. Esto está influenciado por varios factores de solubilidad. Éstos son algunos de los factores de solubilidad.
1. Temperatura
El nivel de temperatura de la solución afecta el proceso de disolución del soluto. A temperaturas más altas, el soluto se disolverá fácilmente en el solvente.
Esto ocurre porque las partículas sólidas a temperaturas más altas se mueven más rápido, lo que permite colisiones más frecuentes y efectivas.
2. El tamaño del soluto
Cuanto más pequeños sean los gránulos de soluto, más fácil se disolverá en el disolvente. La pequeña cantidad de gránulos de soluto hace que el área de la superficie de la sustancia sea más ancha y se extienda en una solución.
Cuanto mayor sea el área de superficie de la sustancia, más partículas colisionan entre sí. Esto es lo que hace que el proceso de disolución sea más rápido.
3. Volumen de disolvente
El gran volumen del solvente afecta el proceso de disolución de la sustancia. Esto se debe a que cada vez más partículas de disolvente reaccionan con el soluto.
Cuanto más volumen de disolvente se utilice, más rápido será el proceso de disolución del soluto.
4. Velocidad de mezcla
El proceso de disolución será más rápido si agrega el factor de agitación.
Al agitar, las partículas de soluto se mezclan cada vez más con el disolvente de modo que la reacción de disolución sea más rápida que la disolución sin agitar.
Esta es una explicación de la solución y solubilidad junto con el significado, propiedades, tipos y factores. Puede ser útil.
